破局“射箭画靶”误区:浙大TarPass校准AI药物生成方向
近日,浙江大学康玉、侯廷军教授与王極可研究员团队在《Advanced Science》(中科院 1 区 TOP 期刊)发表突破性研究,药学院博士生秦睿、计算机学院本科生陈子杰担任共同第一作者。他们提出的 TarPass 评测框架,不仅揭开了行业迷思的真相,更以科学标尺为 AI 药物生成技术划定了规范化发展路径。

图1:研究背景
理性设计,还是 “射箭画靶”?
在 AI 技术深度赋能药物研发的浪潮中,基于靶标的从头分子生成模型被视为行业 “颠覆性工具”—— 它有望大幅缩短研发周期、降低试错成本,破解传统药物发现效率低下的核心瓶颈。
然而,一个根本性的质疑始终悬而未决:这些模型的亮眼性能,是源于真正的靶标理性设计,还是陷入了 “先射箭后画靶” 的德州神枪手谬误?即通过海量生成分子后筛选少量合理案例,人为夸大技术价值。
作为 AI 制药的核心技术,基于靶标的从头分子生成旨在直接设计靶点特异性分子,无需依赖化合物库筛选。
近年来,非 3D、3D “原位生成” 及优化方法三大范式的模型层出不穷,但落地困境持续凸显:模型虽能生成理论上匹配的分子,却难以转化为有效候选药物。其症结在于 —— 缺乏统一、贴近真实药物发现场景的评测标准,导致模型性能无法横向对比,优势常局限于 “事后解释”,行业一度陷入 “虚假繁荣” 的漩涡。
TarPass 框架,建立行业标尺
浙大团队的突破在于构建了首个系统化、可复现的评测标准。TarPass 框架从真实药物研发视角出发,完成了三重关键创新:
• 靶点集科学构建:整合 18 个具有药学代表性的靶点(覆盖激酶、非激酶酶、GPCR 及核受体等关键类别),补充 2 个靶点的 apo 结构,形成包含 20 个蛋白的测试集;
• 数据精准标注:每个靶点均经人工整合晶体结构、文献中的关键相互作用及实验验证的活性数据,严格规避与训练集的交集;
• 多维量化评估:通过 MoleEval(分子性质评估)与 DockEval(构象与相互作用评估)双模块协同,对 15 个代表性模型进行标准化测试,全面揭示各模型的性能差异。
这一框架彻底打破了 “零散评测” 的乱象,为行业提供了可量化、可对比的 “标尺”。
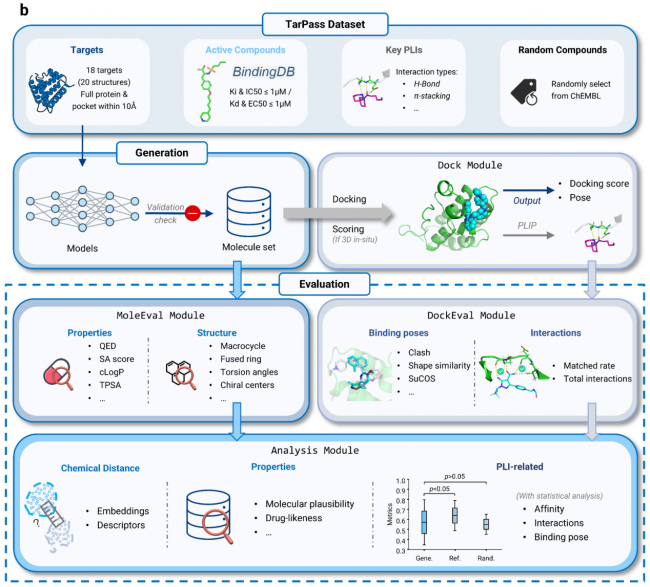
图2:结果与讨论
戳破泡沫,直指优化方向
TarPass 的全面评估结果直指行业痛点:
• 3D “原位生成” 模型优势有限:虽因利用口袋几何信息,性能略优于非 3D 模型,但整体提升并不显著;
• 多数模型性能堪忧:仅少数模型能在多数靶标上超越随机基线,绝大多数模型(含 3D in situ 模型)在关键蛋白 - 配体相互作用(PLIs)恢复率上接近甚至劣于随机基线;
• 典型缺陷集中显现:生成分子存在结构不合理、化学空间偏离类药区间、难以区分结构相近靶点等问题。
这一结果证实:当前多数模型并未实现真正的靶标理性设计,部分宣称的 “技术突破” 实为 “事后筛选美化”,陷入了 “射箭画靶” 的误区。行业长期存在的盲目乐观泡沫被彻底戳破。
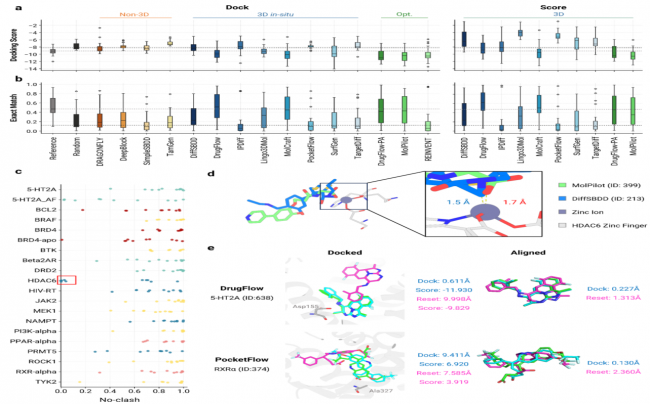
图3:分子合理性和化学空间距离度量
后处理流程,推动技术落地
该研究不仅敢于 “揭短”,更提供了可操作的解决方案。团队设计了多层级虚拟筛选后处理流程,采用 “硬筛选 + 软筛选” 的两阶段策略:
• 将候选分子池缩减至原规模的 10% 以内;
• 有效富集兼具高亲和力与结构相似性的分子;
• 显著提升模型在实际药物发现中的可用性。
尽管经筛选后的分子尚未达到强先导化合物的标准,但该路径为破解 “生成易、落地难” 的行业困境提供了关键范式,推动 AI 分子生成技术从 “理论可行” 迈向 “实际可用”。
校准方向,加速产业化进程
TarPass 框架的深层价值在于重塑行业发展生态:
• 打破 “各自为战” 困局:建立统一评测标准,使不同模型的性能具备横向可比性;
• 精准指引优化路径:研究者可依托该框架精准定位模型短板,聚焦分子预训练、生物物理先验引入等核心方向开展优化;
• 驱动行业良性循环:其开源性与可扩展性将推动行业形成 “评测 - 优化 - 迭代” 的闭环,加速技术产业化落地。
正视短板,释放技术真实潜力
浙大团队的研究传递了一项关键行业共识:AI 分子生成技术并非 “万能钥匙”,目前仍处于发展初级阶段,但在补充化学空间、挖掘潜在活性分子方面具备不可替代的价值。通过 TarPass 标尺的校准、针对性后处理流程的优化,其技术潜力可被充分释放。该研究既不回避现存问题,也不盲目夸大技术价值,为行业注入了理性发展的动能。
里程碑式突破,引领行业新纪元
这项发表于顶刊的研究,是 AI 制药领域的里程碑事件。它不仅破解了长期悬而未决的评测难题,更以科学实证为行业 “校准方向”—— 推动 AI 分子生成技术从 “理论幻象” 走向 “实用加速器”。
随着 TarPass 框架的广泛应用与后续模型的持续迭代,AI 药物生成技术有望摆脱 “理论美好、实际脱节” 的困境,真正成为攻克疑难疾病、研发创新药物的核心引擎,为人类健康事业注入新的动能。(秦炳煜)












