深圳大学张晗/高丽大学Jong Seung Kim/中科院新疆理化所陈挚:铋烯纳米平台“热触发”CRISPR抑制HSP70,破解温和光热耐受
在激光与纳米生物技术交叉领域,温和光热(约42–46°C)被认为更具临床可接受性,但其疗效常被生物学反制机制所限制:肿瘤细胞会迅速启动热休克应答,尤其HSP70显著上调,形成热耐受(thermotolerance),从而削弱温和加热的杀伤效率。简单追求更高温度虽然能增强损伤,却可能带来更大的非靶组织风险。因此,如何在低热剂量、可控温区内突破热耐受,是激光新应用中的关键科学问题。
近日,深圳大学物理与光电工程学院张晗团队、韩国高丽大学化学院Jong Seung Kim团队与中国科学院新疆理化技术研究所陈挚团队合作,提出一种热触发—基因编辑—再增敏光热的闭环策略:以二维铋烯(bismuthene)为光热核心构建多功能核壳纳米平台,把温和光热从“物理加热”升级为可控的“生物触发信号”,在温和加热条件下触发并增强CRISPR/Cas9基因编辑,进而从分子层面削弱肿瘤热耐受防线,使温和光热也能获得显著抑瘤效果。相关成果以“Bismuthene-Based Nanoplatform for Synergistic Thermogenetic CRISPR and Photothermal Cancer Therapy”为题发表于国际权威学术期刊Nano Letters。
该研究的技术亮点在于:并非将光热材料与CRISPR简单叠加,而是构建了可耦合放大的闭环机制。研究团队设计核壳结构纳米平台:以铋烯纳米盘作为高效光热转换核心,外层引入Mn-ZIF壳层实现核酸载荷封装与酸/热响应释放,并通过透明质酸(HA)修饰提升肿瘤微环境中的细胞摄取与递送效率,同时为MRI等成像拓展提供可能,体现出材料与生物技术深度融合的平台化特征。
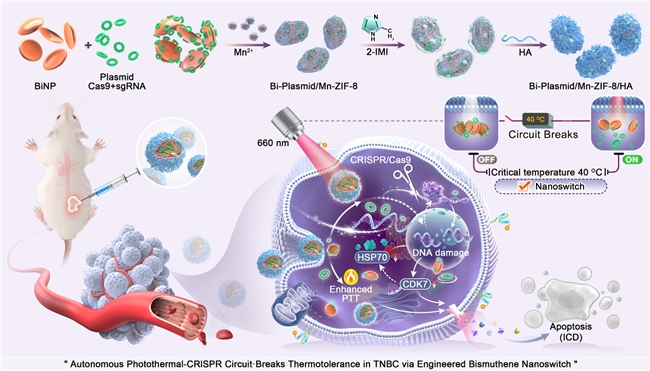
图1 铋烯纳米平台的热触发CRISPR—再增敏光热闭环机制示意图。铋烯纳米盘在激光照射下产生温和热输入,促进Mn-ZIF壳层释放CRISPR/Cas9质粒并增强编辑;CDK7被编辑后抑制HSP70热耐受通路,使后续温和光热在低热剂量下实现更强抑瘤效应。
在机制层面,团队选择CDK7作为CRISPR编辑靶点,利用其在转录调控与细胞应激网络中的上游节点作用,通过编辑诱导DNA损伤响应并选择性抑制HSP70表达,从而降低肿瘤细胞对热刺激的耐受阈值。简言之:第一次温和加热不仅产生直接光热效应,更关键的是促进平台释放并提升细胞内编辑效率;随后CDK7被有效编辑,下游HSP70“热防御”被削弱;在此基础上,相同温度窗口内的后续光热即可触发更强的肿瘤细胞死亡。该闭环使温和光热从“加热杀伤”升级为“可编程调控细胞应激的激光生物开关”。
研究在多项关键实验中验证了策略有效性:体外实验显示,优化sgRNA可实现约57%的CDK7敲低,并伴随DNA损伤信号增强;同时HSP70显著下调而HSP90变化不明显,提示其更偏向“指向性拆解热耐受关键通路”,而非粗放抑制全部热休克蛋白。在动物模型中,热触发CRISPR与温和光热联用组实现>93%的肿瘤抑制;肿瘤组织层面观察到更强的CDK7下调(约87%)与HSP70下调(约88%),且主要脏器病理与血生化指标未见明显异常,显示出较好的生物安全性基础。
该工作为“激光+生物技术”的新应用提供了可推广的设计范式:以二维材料作为高效光热核心,将激光热输入用作可控触发信号,驱动CRISPR等可编程生物工具对关键应激通路实施“热耐受拆解”,从而在更低热剂量、更可控温区内实现更强疗效。未来,随着递送方式、全身给药与长期安全性等问题的进一步验证,该类“热遗传(thermogenetic)”纳米平台有望为精准、低副作用的激光生物医学应用打开新的技术路线。
作者信息: 中科院新疆理化所陈挚研究员、深圳大学林惠玲(博士生)、韩国高丽大学Changyu Yoon(博士生)、深圳大学黄浩副研究员为本文共同第一作者;深圳大学张晗教授(国家优青)、高丽大学Jong Seung Kim教授(韩国科学院院士)、中科院新疆理化所陈挚研究员(海外优青)为本文共同通讯作者;该工作得到了新疆领军人才引进计划、韩国国家研究基金会(NRF)、广东省科技厅、深圳市科创局等的资助。(作者:王霞)












